| 摘 要: | 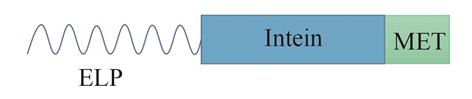
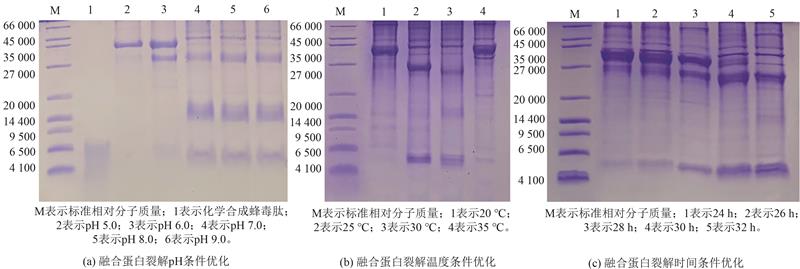
蜂毒肽(Melittin,MET)是一种具有抗炎和抗肿瘤作用的小分子活性肽,其可溶性表达和无融合标签活性肽的纯化一直是个难题。基于类弹性蛋白(Elastin-like polypeptide, ELP)的相变特性和内含肽(Intein)的自裂解特性,构建重组表达菌株Escherichia coli/pET21a-ELP-Intein-MET,在E. coli BL21(DE3)宿主细胞中实现融合蛋白的可溶性表达。重组菌破碎上清液经过温度诱导的可逆相变循环纯化以及融合蛋白自裂解的pH、温度和时间优化,在pH 7.0、30 ℃的条件下自裂解32 h,再经过凝胶层析纯化,得到了纯度高于95%的无融合标签的蜂毒肽。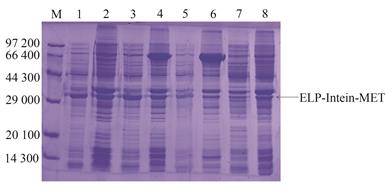
纯化后的蜂毒肽用于Staphylococcus aureus、Bacillus subtilis 168和Escherichia coli JM109的抑菌研究,发现其对革兰氏阳性菌的抑制作用强于革兰氏阴性菌,蜂毒肽在3种菌中的最小抑菌质量浓度分别为12.5、50.0、100.0 μg/mL。作者通过引入弹性蛋白和内含肽,不仅实现了蜂毒肽的高效可溶性表达,且通过较简便的蛋白质分离纯化获得无融合标签的蜂毒肽,该纯化活性肽的抑菌功能与商品化的蜂毒肽相似,有望为蜂毒肽的工业化制备提供新的思路。
|



